Solidžiai į JAV rinką įžengusio medicinos startuolio vadovas: svarbiausia – rasti sprendimą, kuris reikšmingai keistų kasdienę klinikinę praktiką
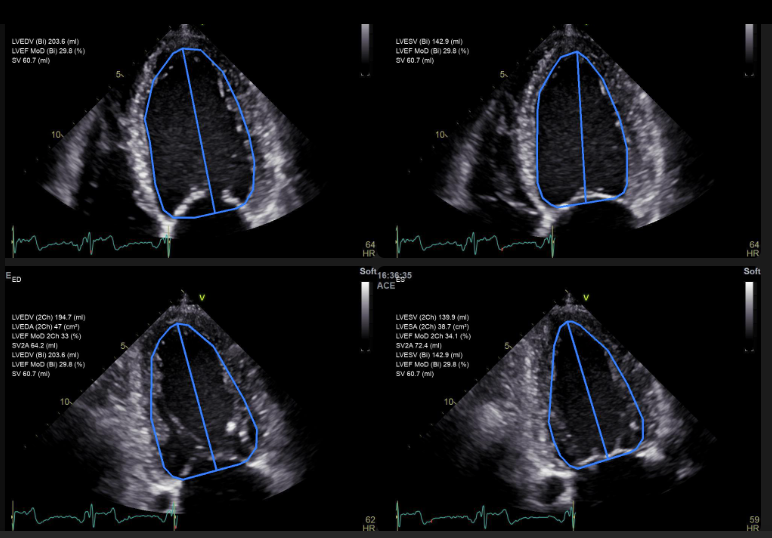
Lietuvos medicinos technologijų (medtech) įmonė „Ligence“ gavo JAV Maisto ir vaistų administracijos FDA 510(k) patvirtinimą dirbtiniu intelektu (DI) paremtai širdies echoskopijos programinei įrangai “Ligence Heart”. FDA yra sveikatos apsaugos institucija ir reguliavimo įstaiga, užtikrinanti sveikatos produktų bei medicinos prietaisų veiksmingumą ir saugumą bei turinti teisę suteikti leidimą parduoti medicinos prietaisus JAV rinkai.
Tai vienas pirmųjų tokio tipo FDA patvirtinimų Centrinės, Šiaurės ir Rytų Europos regionuose širdies ultragarso tyrimų automatizavimui, pasitelkiant dirbtinį intelektą.
Gavus FDA patvirtinimą, JAV sveikatos priežiūros įstaigos nuo šiol galės naudoti „Ligence Heart“ automatinei širdies matavimų analizei ir struktūruotų ataskaitų generavimui. Šis produktas sukurtas siekiant sumažinti gydytojų atliekamų rankinių matavimų apimtį, užtikrinti matavimų nuoseklumą ir pagreitinti echoskopijos procesą, kuris daugybėje klinikų dėl rankinių matavimų yra labai imlus laikui.

Koks buvo „Ligence“ kelias iki šio solidaus pripažinimo JAV? Kokius reikalavimus kėlė FDA?, – paklausėme „Ligence“ bendraįkūrėjo ir direktoriaus, gydytojo kardiologo Arno Karužo. Mūsų pašnekovas taip pat – Lietuvos sveikatos mokslų universiteto (LSMU) MA Kardiologijos instituto Kardiologinių tyrimų automatizacijos laboratorijos jaunesnysis mokslo darbuotojas, projekto „SustAInLivWork“ LSMU dalies vienas iš koordinatorių.
A.Karužas: Jungtinių Amerikos Valstijų (JAV) Maisto ir vaistų agentūra sertifikuoja, vertina įvairius aukštesnės rizikos produktus arba, kaip mūsų atveju, programinę įrangą: ar tokie produktai gali įeiti į JAV rinką ir būti naudojami kasdienėje klinikinėje praktikoje.
Kelias iki šio solidaus pripažinimo buvo sudėtingas. Turėjome pristatyti klinikinius įrodymus, daug įvairios dokumentacijos, įrodančios, kad „Ligence Heart“ programinė įranga bus pakankamai saugi, veiksminga ir tiksli naudoti ją kasdienėje klinikinėje praktikoje su pacientais.
Teko įrodyti konkrečius „Ligence Heart“ privalumus: kad produktas sukurtas pagal visus reikalavimus, atitinka kibernetinės saugos, tikslumo, atvirumo, atkartojamumo ir įvairius kitus kriterijus. Vėliau mūsų programinė įranga buvo testuojama JAV klinikiniuose centruose su įvairiomis pacientų populiacijomis, į šiuos tyrimus buvo įtraukti ekspertai. Klinikinių tyrimų metu tirta, ar dirbtiniu intelektu (DI) grįsti matavimai pakankamai saugūs, tikslūs, ar pasiekia eksperto lygį ir gali būti naudojami kasdienėje klinikinėje praktikoje.
To pavyko pasiekti: įrodėme, kad tam tikri „Ligence Heart“ procesų funkcionalumai, matavimai, kaip, pavyzdžiui, kairiojo skilvelio išstūmio frakcija – vienas iš kertinių parametrų vertinti, ar yra širdies nepakankamumo požymių – praėjo vadinamuosius slenkstinius tikslumo įverčius.
Visi šie duomenys kartu su kibernetinės saugos ir kitais bendraisiais reikalavimais pateikti vertinti FDA – ir tada jau vyko pats vertinimo procesas, buvo teikiami papildomi klausimai, tikslinimai. Taip pat atskirai buvo atlikti testavimai su JAV naudotojais – gydytojais kardiologais, ultragarso technologais: jie išbandė „Ligence Heart“ ir įsivertino, ar gali naudotis šia programine įranga, ar ji patikima.
Po visų klinikinių tyrimų, testavimų organizacija priėmė sprendimą. Labai džiugu, kad šioje srityje tapome pirmieji gavę tokį sertifikatą visame Šiaurės, Centrinės ir Rytų Europos regione. FDA patvirtinimas atveria duris mūsų startuoliui pilnai įeiti į JAV sveikatos sektoriaus rinką.
Kokia yra ši rinka?
JAV apskritai yra viena prioritetinių rinkų – į ją žvelgia daugelis pasaulio startuolių ir įmonių, kadangi tai labai didelė ir labai konkurencinga, itin stipriai pasirengusi inovacijoms rinka, kuri turi didžiulę žmonių populiaciją ir daug investuoja į sveikatos sektorių.
Širdies ultragarso srityje visame pasaulyje yra vos keletas kompanijų, kurios tiesiogiai dirba su širdies ultragarsinio tyrimo automatizacija naudojant DI. Tad visoje šimtamilijoninėje JAV rinkoje esame tretieji, kurie į ją įžengėme su FDA sertifikatu, ir mūsų „Ligence Heart“ gali būti naudojama JAV kasdienėje klinikinėje praktikoje.
Kokias tendencijas matote, ką galėtumėte patarti kitiems sveikatos priežiūros sektoriaus startuoliams?
Sričių, plėtojančių DI pagrįstus radiologinius sprendimus, medicinos srityje šiuo metu išties labai daug, tad labiausiai skatinčiau žengti ne tik į bendrosios radiologijos sritį, bet veikiau į specifines DI pagrįstas tam tikrų ligų diagnostikos sritis: joms pasaulyje skiriama labai daug dėmesio ir nemažai investicijų. Kita itin perspektyvi sritis – vaistų kūrimo procesai, molekulių kūrimas naudojant DI.
Svarbiausia – rasti tokį sprendimą, kuris išties reikšmingai keistų kasdienę klinikinę praktiką ir pilnai į ją įsilietų. Regis, paprasta – tačiau to pasiekti sudėtinga, neretai tenka ilgai testuoti, kol atrandi, kaip galimas sprendinys, inovacija galėtų įsilieti į klinikinio darbo procesą ir jį reikšmingai pakeisti.
Nes yra daug sprendinių, kurie malonūs turėti, bet nėra esminiai, ne tie, kuriuos būtų galima pavadinti „game changers“. Produktus, kurie sukeltų perversmą kasdienėje rutinoje, sukurti sudėtinga, bet jei pavyksta tai padaryti – tai yra didžiulė sėkmė tiek to sprendimo kūrėjams, tiek ir naudotojams – pacientams, medicinos personalui.
Kokie ateities planai?
„Ligence“ siekia, kad aukštos kokybės širdies ultragarso tyrimai būtų prieinami ne tik specializuotuose kardiologijos centruose, bet ir kitose medicinos srityse, kuriose echoskopija tampa vis aktualesnė. Automatizavimas mažina diagnostikos variabilumą ir sudaro galimybes greičiau pastebėti širdies funkcijos pokyčius.
Įmonė planuoja tęsti plėtrą JAV ir Europos rinkose plėsdama „Ligence Heart” produkto funkcionalumą, siekdama naujų 510(k) patvirtinimų bei didindama suteikiamą klinikinę vertę.
Pagrindiniai startuolio prioritetai dabar yra Europos ir JAV rinkos. Įdomios ir gretutinės rinkos – Kanados, Japonijos, Pietų Korėjos. Pradėtų klinikinių tyrimų jau turime ir Australijoje.
Džiugu, kad nuo pasaulinio spartaus ritmo DI plėtros medicinos srityje neatsiliekame ir Lietuvos sveikatos mokslų universitete (LSMU). Neseniai „European Heart Journal Digital Health“ žurnale publikuotas mokslo straipsnis su DI sprendimu krūvio echokardiografijos pritaikymui – tai pirmasis lietuvių autorių straipsnis šiame aukšto lygio žurnale.
LSMU prisijungė ir drauge su kitais universitetais iš Lietuvos (KTU, Vilnius Tech bei VDU) bei tarptautiniais partneriais aktyviai dalyvauja dideliame Kauno technologijos universiteto koordinuojamame projekte „Dirbtinio intelekto ekscelencijos centras tvariam vystymuisi“ – „SustAInLivWork“ (angl. Centre of excellence of artificial intelligence for sustainable living and working).
„SustAInLivWork“ kompetencijos centras stiprina šalies mokslininkų ir tyrėjų mokslinių tyrimų bei inovacijų kompetencijas kuriant ir vystant dirbtinio intelekto (DI) sprendimus. Projekto veiklos teikia galimybių skaitmenizuoti Lietuvos gamybos, sveikatos, transporto ir energetikos sektorius, skatina mokslinių tyrimų, eksperimentinės plėtros ir inovacijų plėtrą taikant DI technologijomis grįstus sprendimus, reikšmingai prisidės stiprinant Lietuvos konkurencingumą tarptautiniu mastu.
LSMU jau vyksta nauji doktorantų moksliniai darbai DI pritaikymui medicinoje. Vienas pirmųjų netrukus ginsiu šios srities disertaciją – džiugu, kad su įvairiais DI sprendiniais jau dirba ir daugiau LSMU doktorantų ir mokslininkų.
